今日���,美國FDA宣布,已授予輝瑞的口服抗新冠病毒藥物Paxlovid緊急使用授權(quán)(EUA)����,用于治療輕度至中度的新冠疾病患者。FDA官方新聞稿指出���,這是首款獲其授權(quán)治療新冠疾病的口服抗病毒藥物����。
“今日的授權(quán)帶來了第一款以藥片形式口服的新冠療法�,這是對(duì)抗這場全球流行病的重要一步,”美國FDA藥品評(píng)估與研究中心的Patrizia Cavazzoni主任說道�����,“這項(xiàng)授權(quán)在全新變種出現(xiàn)的關(guān)鍵時(shí)刻���,帶來了抗擊新冠的全新工具,也讓有高風(fēng)險(xiǎn)發(fā)展為新冠重癥的患者能更容易獲得抗病毒療法����?����!?/span>Paxlovid由兩種主要成分組成:nirmatrelvir(PF-07321332)是一種新冠病毒3CL蛋白酶抑制劑��,能通過阻斷新冠病毒3CL蛋白酶的活性����,破壞新冠病毒的后續(xù)RNA復(fù)制過程�。另一種成分ritonavir則讓nirmatrelvir能在身體里保持更長時(shí)間的活性,更好地抗擊病毒����。
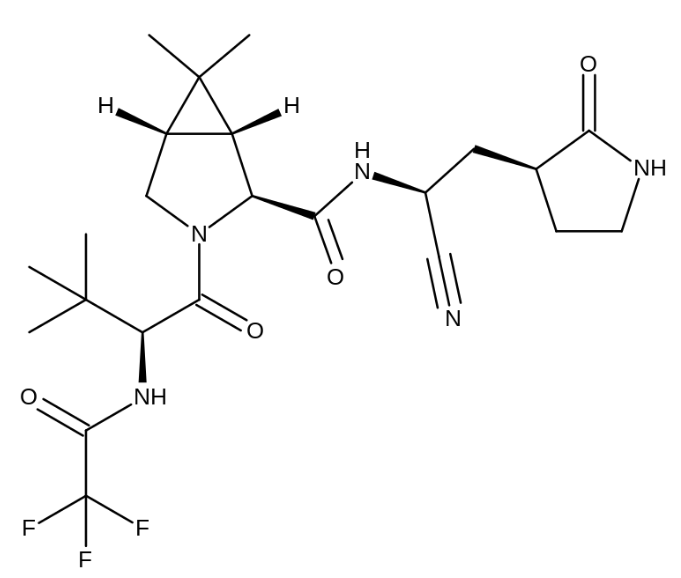
▲Nirmatrelvir分子結(jié)構(gòu)式(圖片來源:Michael D. Turnbull, CC BY-SA 4.0 <https://creativecommons.org/licenses/by-sa/4.0>, via Wikimedia Commons)支持這一緊急使用授權(quán)的數(shù)據(jù)主要來自一項(xiàng)隨機(jī)、雙盲�����、安慰劑對(duì)照的臨床試驗(yàn)���。該試驗(yàn)招募了確診新冠陽性���,尚未住院��,但出現(xiàn)癥狀的成人患者。這些患者之前均未接受新冠疫苗注射����,也從未感染過新冠。FDA的新聞稿中提到����,臨床試驗(yàn)數(shù)據(jù)表明����,Paxlovid能顯著降低患者新冠相關(guān)住院或全因死亡的風(fēng)險(xiǎn)。與安慰劑對(duì)照組相比��,Paxlovid組中出現(xiàn)住院或死亡的患者比例減少了約88%(治療組0.8%��,安慰劑對(duì)照組6%)�����。此外,安慰劑對(duì)照組中有9名患者死亡���,而治療組的數(shù)據(jù)為0名���。目前�����,Paxlovid治療新冠的安全性和有效性還在接受進(jìn)一步的評(píng)估。FDA的新聞稿中提到,適用這款藥物的人群有著限制�����。他們需不小于12歲���,體重不低于40公斤,且新冠病毒直接檢測的結(jié)果為陽性�����。這些患者有較高風(fēng)險(xiǎn)發(fā)展為重癥新冠疾?�。ㄈ缱≡夯蛘咚劳觯?�。這是一款處方藥����,可在新冠確診,且在癥狀出現(xiàn)的五天內(nèi)盡快使用�。FDA同樣指出����,Paxlovid的授權(quán)并不包括新冠暴露前后的預(yù)防,也不包括危重癥新冠患者的治療���。Paxlovid并不能代替疫苗�����。同時(shí)�����,緊急使用授權(quán)也不等同于FDA的完整批準(zhǔn)�。

藥明康德內(nèi)容團(tuán)隊(duì)制圖
“今日Paxlovid的批準(zhǔn)再次展示科學(xué)能如何幫助我們最終打敗疫情���。盡管已經(jīng)發(fā)生了兩年��,這場疫情依舊影響著全球人們的生活�����。這款具有突破性的療法能顯著減少住院和死亡風(fēng)險(xiǎn),也能在家服用�,能改變我們治療新冠疾病的方式����。我們希望它能減少一些醫(yī)療體系面臨的重大壓力��?��!陛x瑞首席執(zhí)行官Albert Bourla博士說道。回溯過往,這款創(chuàng)新療法的研發(fā)歷史還要從2002年說起�����。那時(shí)�����,輝瑞的研發(fā)人員為了應(yīng)對(duì)SARS病毒(SARS-CoV-1)����,著手尋找3CL蛋白酶抑制劑,從而發(fā)現(xiàn)了nirmatrelvir的前體PF-00835231���,在體外實(shí)驗(yàn)中���,它能夠強(qiáng)力抑制SARS-CoV-1的3CL蛋白酶活性��。在新冠疫情爆發(fā)后�����,科學(xué)家們馬上想到了這款在研化合物���,因?yàn)镾ARS病毒和新冠病毒的3CL蛋白酶在與底物結(jié)合的位點(diǎn)上具有100%的序列同源性����,這意味著nirmatrelvir很可能對(duì)新冠病毒的3CL蛋白酶具有強(qiáng)力的抑制效果。后續(xù)的實(shí)驗(yàn)也證明了這一點(diǎn)�。

圖片來源:123RF
不過,最初發(fā)現(xiàn)的這款化合物不能口服使用���,面對(duì)新冠疫情的迅速擴(kuò)展�,研究人員馬不停蹄��,對(duì)它進(jìn)行了優(yōu)化��,生成了PF-07321332,也就是后來的nirmatrelvir����。根據(jù)行業(yè)媒體《C&EN》的報(bào)道����,2020年7月,科學(xué)家們首次合成了7毫克的化合物����。但要在人體中進(jìn)行臨床試驗(yàn),7毫克的化合物是遠(yuǎn)遠(yuǎn)不夠的��。輝瑞公司的210名科學(xué)家通力合作����,到10月份���,他們已經(jīng)合成了100克的化合物,兩周之后�����,化學(xué)家們將合成能力提高到超過1000克�����。科學(xué)家們的努力�����,讓nirmatrelvir的臨床試驗(yàn)得以迅速開展�����,也為今日的突破提供了強(qiáng)有力的支持���。新一代口服抗新冠病毒藥物的問世,有望與新冠疫苗�、中和抗體和其它新冠療法一起,為人們提供多重保護(hù)���,有效遏制疫情的發(fā)展。這是屬于科學(xué)的榮光!我們向快馬加鞭����,推動(dòng)新冠藥物開發(fā)的研發(fā)人員致敬��,也深深地感謝那些默默耕耘�,為新冠疫苗和療法的成功奠基的科學(xué)家們。是他們的共同努力��,讓我們早日看到終結(jié)疫情的希望����!
參考資料:
[1] Coronavirus (COVID-19) Update: FDA Authorizes First Oral Antiviral for Treatment of COVID-19, Retrieved December 22, 2021, from https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-authorizes-first-oral-antiviral-treatment-covid-19
[2] Pfizer Receives U.S. FDA Emergency Use Authorization for Novel COVID-19 Oral Antiviral Treatment, Retrieved December 22, 2021, from https://www.businesswire.com/news/home/20211221005795/en





