2022年已經(jīng)到來(lái),在新的一年里�����,生物醫(yī)藥領(lǐng)域有哪些研發(fā)項(xiàng)目值得關(guān)注���?近日��,Evaluate發(fā)布了一份報(bào)告�,對(duì)產(chǎn)業(yè)的2022年發(fā)展進(jìn)行了預(yù)測(cè)�����。昨日�,藥明康德內(nèi)容團(tuán)隊(duì)已經(jīng)介紹了有望在今年獲批的九大潛在重磅療法。在今天的這篇文章里�,我們來(lái)看一看其它值得關(guān)注的八大研發(fā)項(xiàng)目。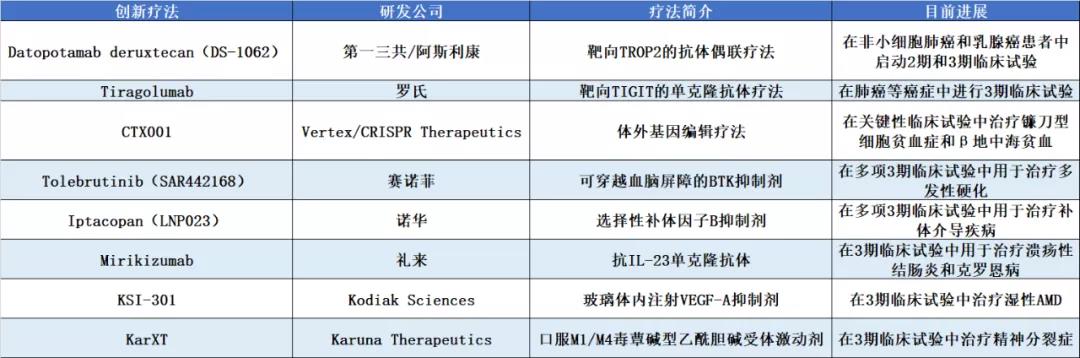
▲2022年值得關(guān)注的八大研發(fā)項(xiàng)目(數(shù)據(jù)來(lái)源:參考資料[1]���,藥明康德內(nèi)容團(tuán)隊(duì)制圖����;點(diǎn)擊圖片可觀看大圖)
Datopotamab deruxtecan(第一三共/阿斯利康)Datopotamab deruxtecan是第一三共和阿斯利康聯(lián)合開發(fā)的靶向TROP2的抗體偶聯(lián)藥物�,在去年進(jìn)行的圣安東尼奧乳腺癌研討會(huì)(SABCS)上公布的臨床結(jié)果顯示����,在接受標(biāo)準(zhǔn)治療后疾病進(jìn)展的三陰性乳腺癌患者中��,datopotamab deruxtecan達(dá)到34%的客觀緩解率(15/44)��,其中包括14名確認(rèn)完全緩解/部分緩解�,另有17名患者在中位隨訪時(shí)間為7.6個(gè)月時(shí)疾病穩(wěn)定。截至2021年7月30日��,疾病控制率為77%�����。它目前在多項(xiàng)2期和3期臨床試驗(yàn)中用于治療乳腺癌和非小細(xì)胞肺癌���。Tiragolumab是羅氏開發(fā)的靶向TIGIT的單克隆抗體療法。TIGIT(T cell immunoreceptor with Ig and ITIM domains)全稱為T細(xì)胞免疫球蛋白和ITIM結(jié)構(gòu)域蛋白���,是主要在T細(xì)胞和自然殺傷(NK)細(xì)胞表面表達(dá)的免疫檢查點(diǎn)蛋白��。用tiragolumab阻斷TIGIT信號(hào)通路�����,有可能增強(qiáng)機(jī)體對(duì)癌細(xì)胞的免疫反應(yīng)���,提高抗腫瘤活性���。去年12月公布的最新臨床試驗(yàn)結(jié)果顯示,在一線治療PD-L1陽(yáng)性轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)患者的2期臨床試驗(yàn)中�,與阿替利珠單抗單藥治療相比,tiragolumab/阿替利珠單抗組合使患者疾病進(jìn)展或死亡的風(fēng)險(xiǎn)降低了38%�。目前,它在多項(xiàng)3期臨床試驗(yàn)中與阿替利珠單抗聯(lián)用��,治療非小細(xì)胞肺癌��、小細(xì)胞肺癌和局部晚期食管癌����。
CTX001(Vertex/CRISPR Therapeutics)CTX001是一種在研自體CRISPR/Cas9基因編輯療法。通過(guò)在體外對(duì)患者的造血干細(xì)胞進(jìn)行改造���,使紅細(xì)胞中產(chǎn)生高水平的胎兒血紅蛋白(HbF)��。HbF是攜帶氧氣的血紅蛋白的一種形式�����,在出生時(shí)自然存在���。通過(guò)CTX001治療����,可以提高HbF水平�,從而緩解輸血依賴性β地中海貧血(TDT)的輸血需求,并減少嚴(yán)重鐮刀型細(xì)胞貧血病患者的疼痛和使人衰弱的血管閉塞性危象����。今年6月,兩家公司公布了22名患者的初步臨床試驗(yàn)數(shù)據(jù)�����,確定了這款療法的潛力�����,使其有望成為治療這兩種疾病的潛在一次性治愈療法���。目前,該試驗(yàn)的1/2期臨床試驗(yàn)已招募完畢��,正在等待后續(xù)結(jié)果。如果一切順利���,這兩家公司有望在2022年向美國(guó)FDA遞交申請(qǐng)�。對(duì)于CRISPR基因編輯技術(shù)����,這可能成為又一項(xiàng)重大突破。

圖片來(lái)源:123RF
Tolebrutinib(曾用名SAR442168)是一款能夠穿過(guò)血腦屏障的口服魯頓氏酪氨酸激酶(BTK)抑制劑����。BTK是B細(xì)胞受體信號(hào)通路的關(guān)鍵組成部分。BTK對(duì)各種免疫細(xì)胞的發(fā)育和功能都很重要�����,包括B淋巴細(xì)胞和巨噬細(xì)胞���。通過(guò)抑制BTK���,可調(diào)節(jié)與大腦和脊髓神經(jīng)炎癥相關(guān)的適應(yīng)性和先天性免疫細(xì)胞。這款BTK抑制劑在治療多發(fā)性硬化患者的2b期臨床試驗(yàn)中已經(jīng)達(dá)到主要和次要終點(diǎn)��。目前,賽諾菲正在進(jìn)行多項(xiàng)3期臨床試驗(yàn)����,在不同類型的多發(fā)性硬化癥患者中檢驗(yàn)它的療效。Iptacopan(LNP023)是一款潛在“first-in-class”的口服選擇性補(bǔ)體因子B抑制劑��。補(bǔ)體信號(hào)通路在多種罕見(jiàn)腎病和血液疾病中起到重要作用��。Iptacopan已經(jīng)在治療IgA腎病和C3腎小球病的2期臨床試驗(yàn)中獲得積極結(jié)果����,也獲得美國(guó)FDA授予的突破性療法認(rèn)定,治療陣發(fā)性睡眠性血紅蛋白尿癥��。
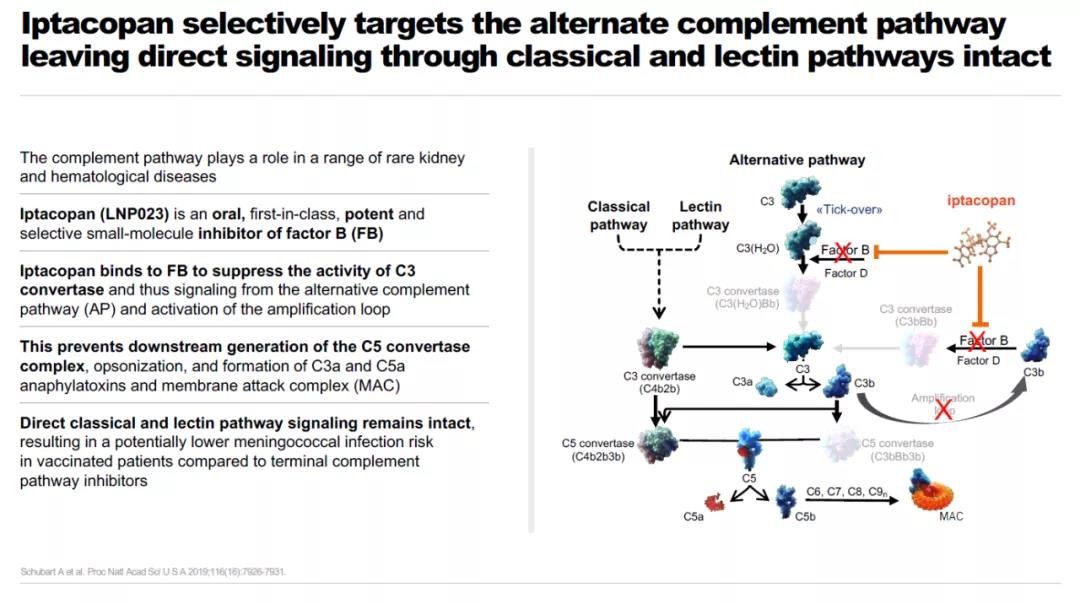
▲Iptacopan簡(jiǎn)介(圖片來(lái)源:諾華公司官網(wǎng))
Mirikizumab是一種人源化IgG4單克隆抗體��,可與IL-23的p19亞基結(jié)合����,阻斷IL-23介導(dǎo)的炎癥反應(yīng)。它在治療中重度潰瘍性結(jié)腸炎的3期臨床試驗(yàn)中已經(jīng)達(dá)到主要和關(guān)鍵性次要終點(diǎn)����,預(yù)計(jì)在2022年上半年遞交監(jiān)管申請(qǐng)。它同時(shí)在3期臨床試驗(yàn)中用于治療克羅恩病���。KSI-301是Kodiak Sciences開發(fā)的一款抗體偶聯(lián)生物聚合物(antibody biopolymer conjugate)�����,它將靶向VEGF-A的單克隆抗體與生物聚合物偶聯(lián)在一起����,顯著延長(zhǎng)了藥物在眼睛中的半衰期���。這意味著它可以延長(zhǎng)兩次眼內(nèi)注射之間的時(shí)間間隔��,減少注射頻率���,提高患者的治療依從性。
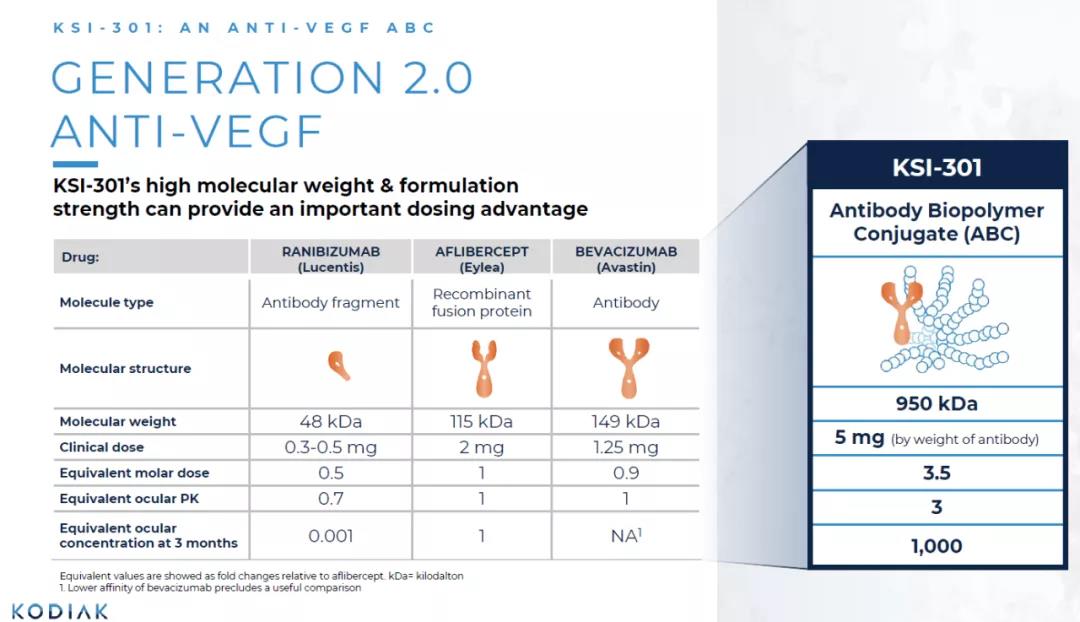
圖片來(lái)源:Kodiak Sciences官網(wǎng)
目前它已經(jīng)完成治療濕性年齡相關(guān)性黃斑變性(AMD)的3期臨床試驗(yàn)的患者注冊(cè)��,并且還在臨床試驗(yàn)中用于治療糖尿病性黃斑水腫���,視網(wǎng)膜靜脈阻塞等眼科疾病患者��。KarXT(Karuna Therapeutics)KarXT由xanomeline和rospium chloride兩種有效成分構(gòu)成�,旨在激活大腦中的毒蕈堿型乙酰膽堿受體的同時(shí)�����,減少對(duì)外周毒蕈堿型乙酰膽堿受體的作用。通過(guò)刺激毒蕈堿受體M1和M4受體���,受體激動(dòng)劑xanomeline可緩解精神分裂癥患者的負(fù)面癥狀�,如冷漠�����、社會(huì)驅(qū)動(dòng)力減少�����。它還可以提高認(rèn)知能力����,并對(duì)改善其它精神癥狀,如幻覺(jué)和妄想很有幫助����。Xanomeline的弱點(diǎn)是其外周膽堿能副作用,導(dǎo)致該藥物耐受性差�����。而季銨鹽化合物trospium chloride為毒蕈堿受體拮抗劑,僅作用于外周神經(jīng)��,不會(huì)進(jìn)入中樞神經(jīng)系統(tǒng)����,因此不會(huì)干擾中樞神經(jīng)系統(tǒng)內(nèi)xanomeline的正常工作����。由于trospium chloride具有較長(zhǎng)的半衰期,它能夠全程抑制外周神經(jīng)中的xanomeline的作用��。值得提及的是�,這兩種藥物經(jīng)不同的肝臟酶代謝,意味著藥物間的相互作用可能更少���。去年11月����,再鼎醫(yī)藥與Karuna Therapeutics就在大中華區(qū)開發(fā)���、生產(chǎn)及商業(yè)化KarXT達(dá)成獨(dú)家許可協(xié)議�。目前���,KarXT在4項(xiàng)臨床試驗(yàn)中用于治療精神分裂癥�,以及阿爾茨海默病患者的精神病發(fā)作。我們預(yù)祝這些創(chuàng)新研發(fā)項(xiàng)目進(jìn)展順利��,為患者早日到來(lái)更好的治療選擇���。
參考資料:
[1] Evaluate Vantage 2022 Preview, Retrieved January 2, 2022, from https://www.evaluate.com/thought-leadership/vantage/evaluate-vantage-2022-preview-report
[2] Datopotamab Deruxtecan Continues to Show Promising Durable Response and Disease Control in Patients with Metastatic Triple Negative Breast Cancer. Retrieved December 10, 2021, from https://www.daiichisankyo.com/files/news/pressrelease/pdf/202112/20211207_E2.pdf
文章來(lái)源:藥明康德






